
各位老师,各位同学,各位“肠·道”好友,大家晚上好!
我是来自北京大学的姜长涛,首先十分感谢热心肠这个平台,为我们提供“肠·道”这个演讲。
今晚我十分荣幸在这里,与大家分享“宿主与菌群共代谢的分子机制”的研究相关进展。

我们人体拥有大量的共生菌,这些共生菌的重量加到一起,大概有1-2公斤,其中95%以上的共生菌是寄居在人体的肠道,叫做肠道菌。
单个肠道菌的体积,比我们人体的体细胞通常都要小,但肠道菌的数量却远多于人体的细胞,大概是人体细胞的10倍。
如此多的肠道菌寄居在我们人体的体内,它并不是来旅游的,而是发挥着十分重要的生理学功能。
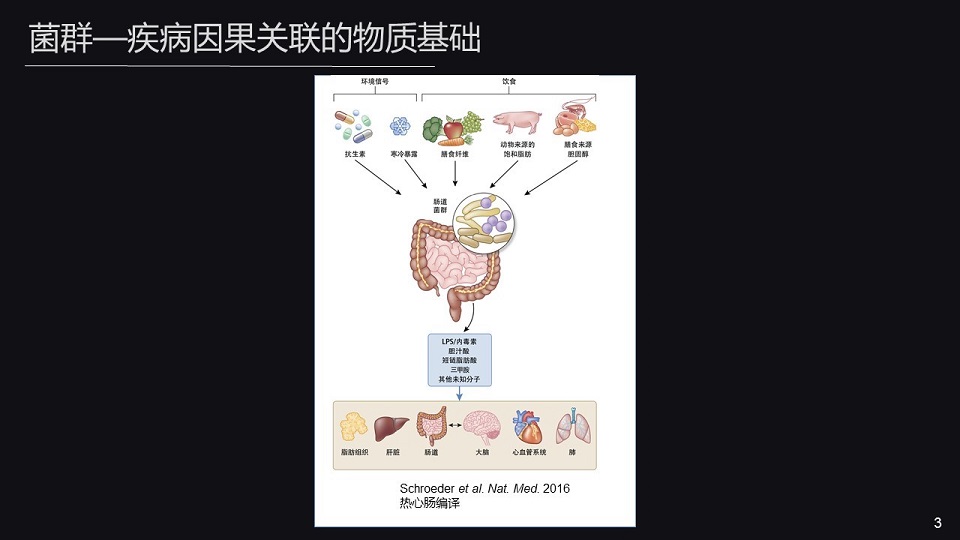
肠道菌是连接宿主与外界环境之间的纽带与桥梁,它能够精确的感知外界信号以及食物当中成分的变化。
肠道菌代谢产生的小分子物质能够作用于宿主的各器官,如脂肪、肝脏、大脑和心血管系统,影响它们的代谢稳态。
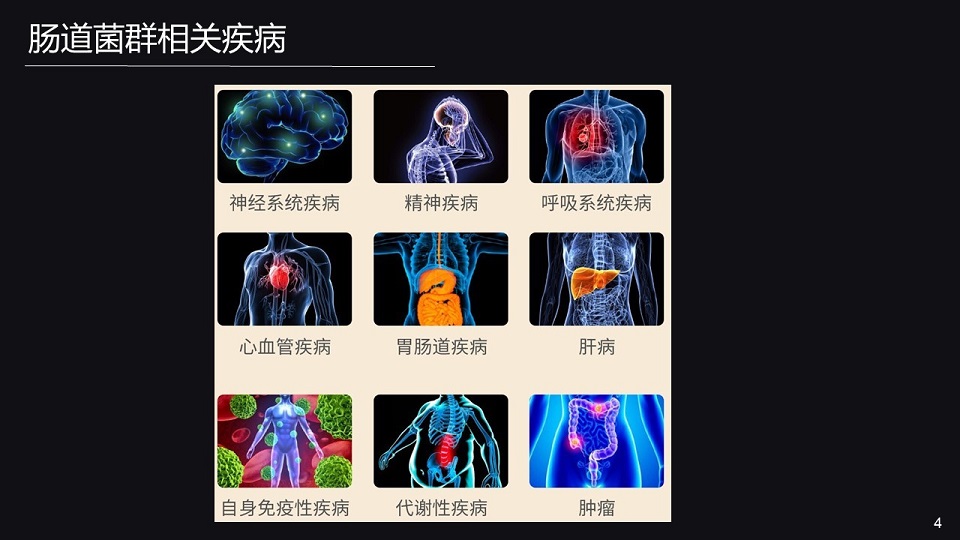
目前已知肠道菌群紊乱与多种疾病密切相关,但目前大多数的研究都是关联性的,缺乏因果关系的建立。
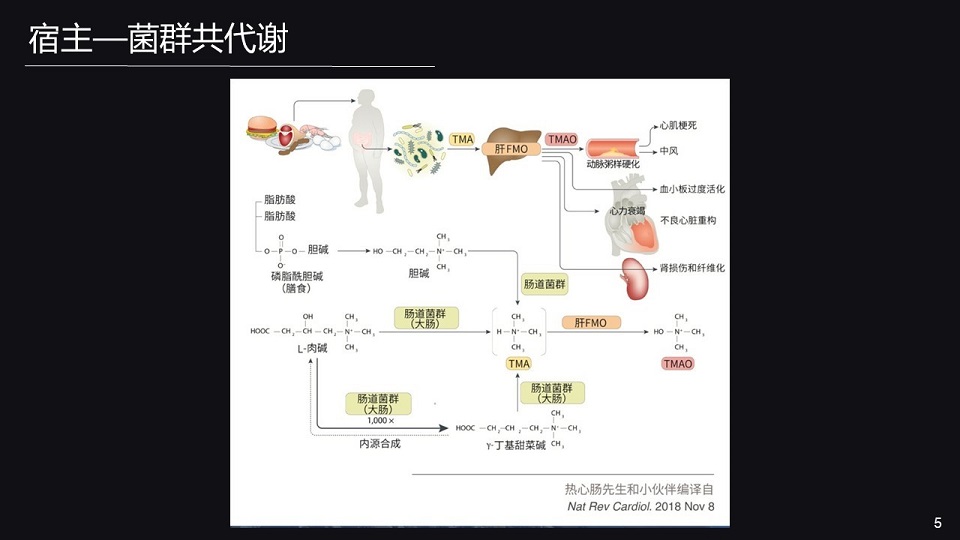
那谈到宿主和肠道菌的共代谢,我在这里想举一个例子。
来源于食物当中的胆碱,在肠道菌的一系列酶的作用下,首先生成三甲胺;三甲胺进入到循环系统,最终到达到肝脏,被肝脏的相关的酶FMO(含黄素单氧化酶)氧化,生成氧化性三甲胺。
氧化性三甲胺对心血管具有非常有害的作用,能进一步诱导心肌梗死、脑卒中甚至是心功能衰竭等。
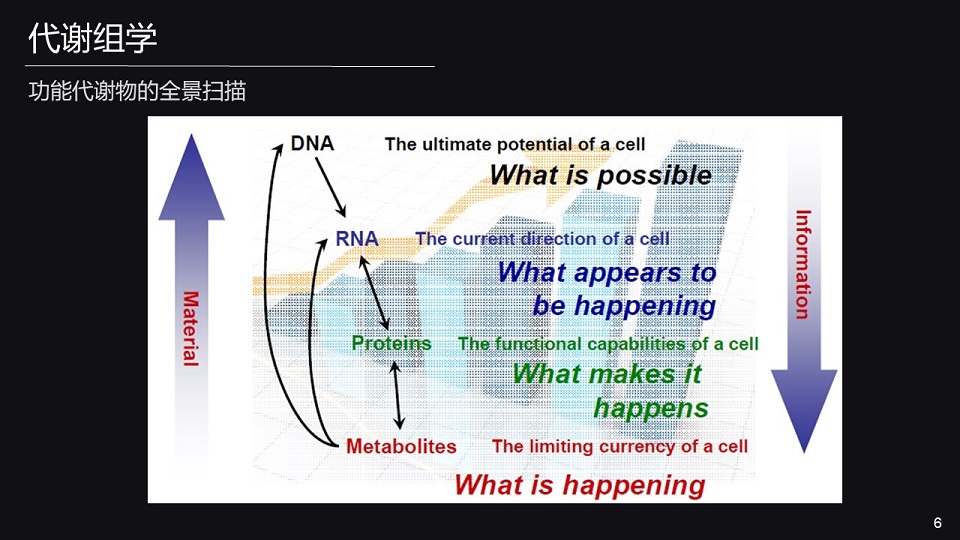
代谢组学是我们肠道研究的一把利器,那么什么是代谢组学呢?主要是针对小分子代谢物的高通量、定性、定量分析的检测方法。
与传统的其它的组学,比如基因组、转录组和蛋白组相比,代谢组学有哪些优势呢?
其它组学主要告诉我们,什么可能会发生,什么将要会发生,什么已经发生了。而代谢组学则告诉我们,此时此刻机体正在进行的代谢改变,它更能如实的反映机体的代谢表型。
那我们主要是应用代谢组学,探寻疾病发展进程当中关键的代谢小分子的动态改变。
再进一步结合宏基因组,向上找到影响这些代谢小分子改变的关键的菌株;向下找到它们在宿主上的关键的靶点。
更为重要的是,我们针对这些靶点,进行相关的候选药物干预研究。
下面我将着重介绍一下我们的系列研究工作。
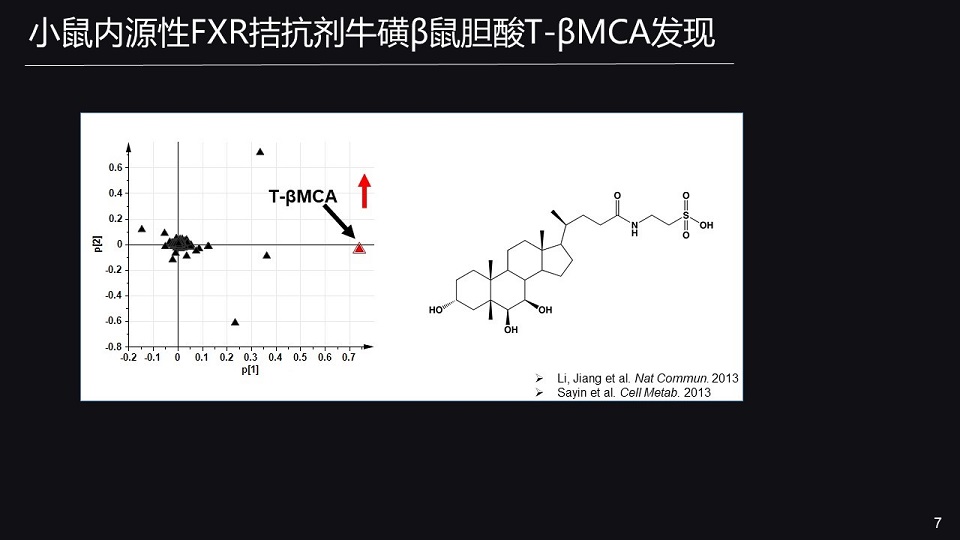
首先,我们基于代谢组学技术,发现无菌小鼠体内的小分子代谢物,跟正常的野生型小鼠相比明显不同。
其中变化最明显的小分子代谢物,被鉴定为牛磺β鼠胆酸(T-βMCA)。那什么是T-βMCA呢?T-βMCA是小鼠内源性胆汁酸的一种。
随后我们发现,伴随着T-βMCA在肠组织的蓄积,无菌小鼠肠核受体FXR(法尼醇X受体)的信号通路明显被抑制。
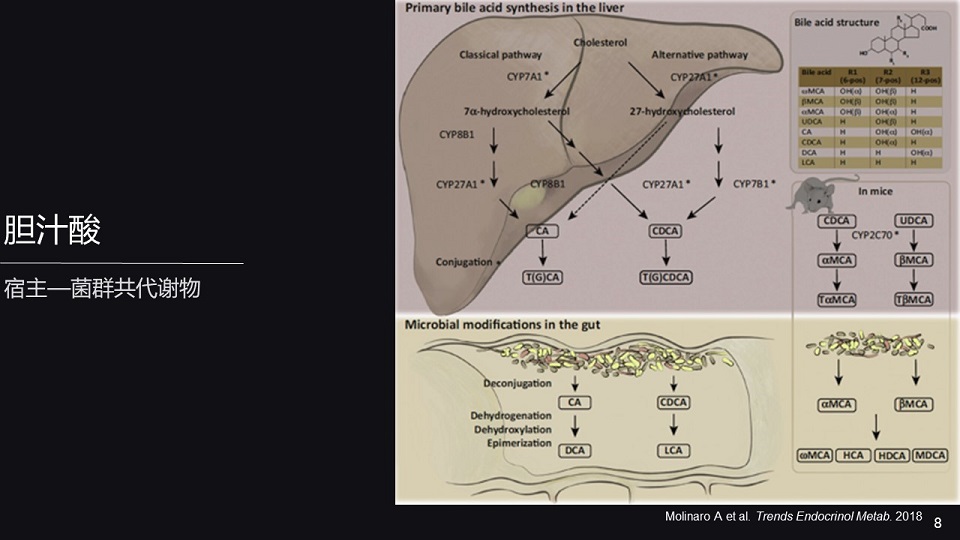
当我们谈到胆汁酸的代谢,它是主要在肝脏当中由胆固醇代谢生成的。
参与其中的酶有几十种,在这些酶当中,最为重要的是胆汁酸生成的限速酶,胆固醇7α-羟化酶CYP7A1。在这个酶的作用下,胆固醇能够生成胆酸(CA)、鹅去氧胆酸(CDCA)。
我们还发现,在小鼠的肝脏表达另外一种关键的酶CYP2C70,在这种酶的作用下,能够代谢CDCA生成鼠胆酸(MCA)。
而我们人体肝脏当中缺少这种酶,所以说在人体内没有MCA。那胆汁酸CA、CDCA、MCA统称为初级胆汁酸。
这些初级胆汁酸在肝脏能进一步的与甘氨酸、牛磺酸螯合生成结和性胆汁酸。结和性胆汁酸储存在胆囊当中,当我们进食的时候,这些胆汁酸能够释放进入到肠道。
在肠道菌的作用下,首先发生水解,变成游离的胆汁酸。这些游离的初级胆汁酸,在肠道菌的进一步作用下,发生去氢化、去羟化和异构化等,产生次级胆汁酸。
这就包括,CA产生脱氧胆酸,CDCA生成石胆酸,MCA生成猪胆酸和猪去氧胆酸。
那肝脏生成的这些胆汁酸进入到肠道,其中95%在小肠的末段回肠被重新吸收进入门静脉系统,最终到达到肝脏,参与到新一轮的胆汁酸的生成。
这一现象,生理学上叫做胆汁酸的肠肝循环,在我们人体,一天肠肝循环大概6-10次。
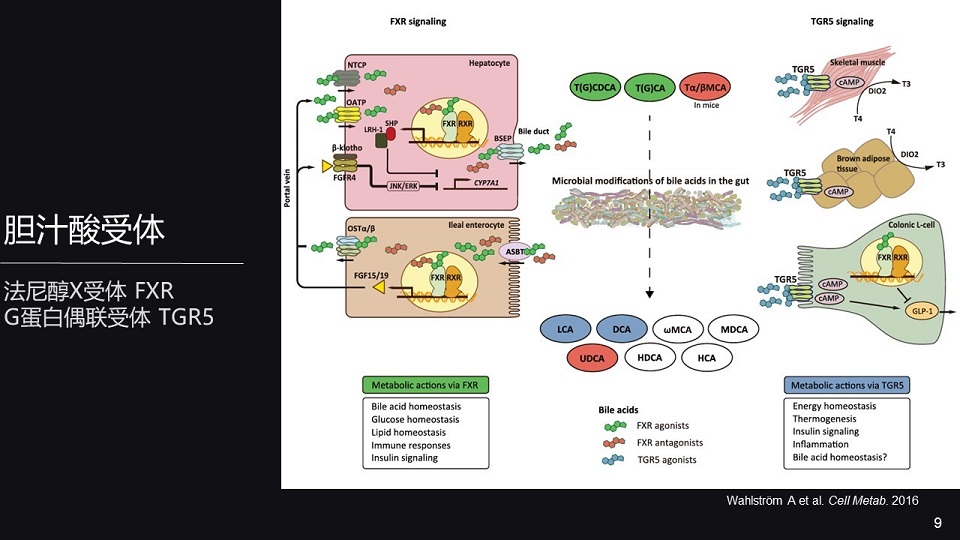
谈到胆汁酸的生理功能,大家都熟知的是能够促进脂质的消化与吸收。随着人们对胆汁酸功能的深入研究,发现胆汁酸还是人体内十分重要的信号分子。
那发挥这个作用主要依赖于两种关键的受体,一种是法尼醇X受体(FXR),它是核受体的一种,另外一种是G蛋白偶联受体(TGR5)。
其中FXR在胆汁酸的代谢当中起到一个负反馈调控作用,具体来说,在肝脏当中,FXR被胆汁酸激活之后,它能够抑制CYP的生成,进一步减少胆汁酸的生成。
那在肠道呢,FXR也能被胆汁酸激活。它一方面能够抑制胆汁酸转运体(ASBT)的表达,从而抑制胆汁酸的重吸收;另外一方面,通过生成FGF-15或者19介导的肠肝对话,间接的通过抑制肝脏的CYP7A1,从而抑制胆汁酸的生成。
那在胆汁酸当中,CDCA和CA是FXR内源性的配体。我们实验室以及其它实验室陆续也发现了,胆汁酸当中有FXR内源性的拮抗剂,如TαMCA和TβMCA。
另外一个,G蛋白偶联受体TGR5,它在代谢当中也发挥着十分重要的作用。
TGR5主要在骨骼肌、棕色脂肪组织和肠道L细胞高表达。TGR5在体内的配体主要是次级胆汁酸,LCA与DCA。
其中在L细胞中,TGR5被激活之后,能够促进GLP-1(胰高血糖素样肽- 1)的生成与释放。
谈到GLP-1呢,大家都熟知。GLP-1的类似物——利那鲁肽目前是临床治疗II 型糖尿病的明星药物。
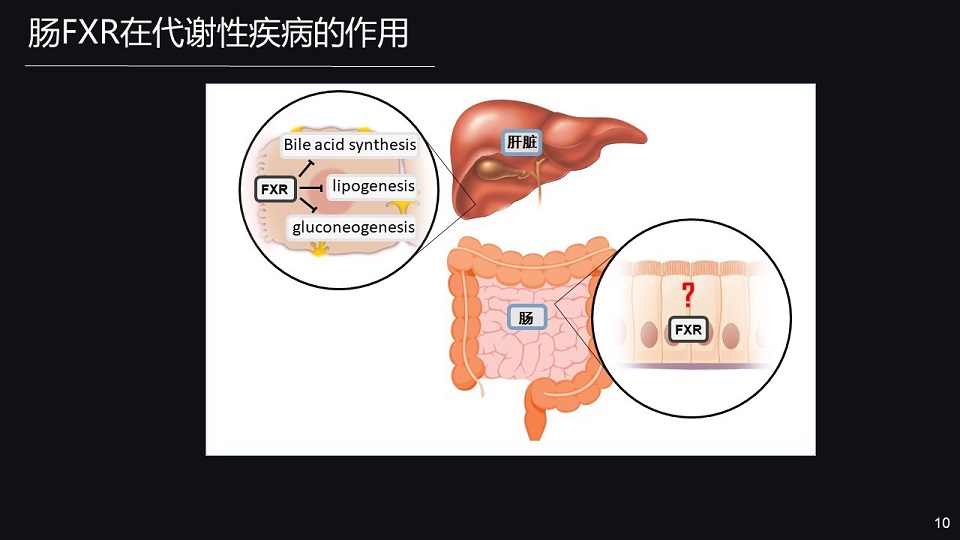
核受体FXR在糖脂代谢的调节中,发挥十分重要的作用,也是重要的药物靶标。
那肝脏FXR被激活之后,它能够抑制胆汁酸的生成,抑制脂质的生成,降低甘油三酯,抑制糖的异生,降低血糖。
那在全身呢,FXR的激动剂并不能有效的改善II 型糖尿病。这就提示其他组织中,FXR对糖脂代谢的调节作用,可能与肝脏完全不同。
那FXR在肠道也是高表达,肠FXR在代谢疾病当中的作用尚不完全清楚。
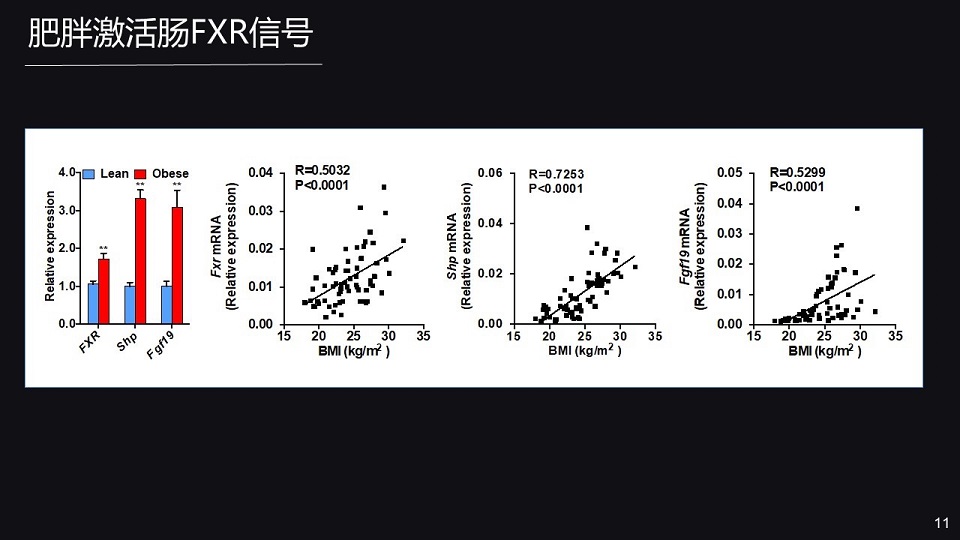
我们实验室对肠FXR的作用进行了深入的探讨。
首先,我们发现对于肥胖的患者,他体内肠FXR的信号显著的激活,但肝FXR的信号没有明显的改变;肠FXR的信号与体重指数BMI呈明显的正相关。
我们进一步呢,在糖尿病的小鼠里也观察到了相似的现象。
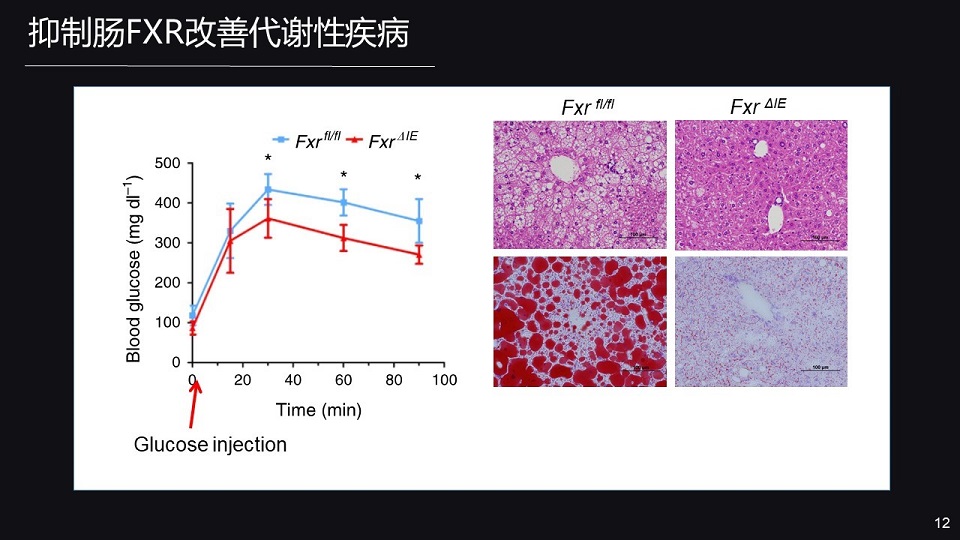
为了进一步深入探讨肠FXR在代谢性疾病当中的作用,我们建立了肠FXR特异敲除小鼠。
我们给予野生型小鼠与肠FXR特异敲除小鼠高脂饮食,我们发现与正常的对照小鼠相比,肠FXR敲除鼠明显能够抵抗高脂饮食诱导的肥胖、胰岛素抵抗与脂肪肝。
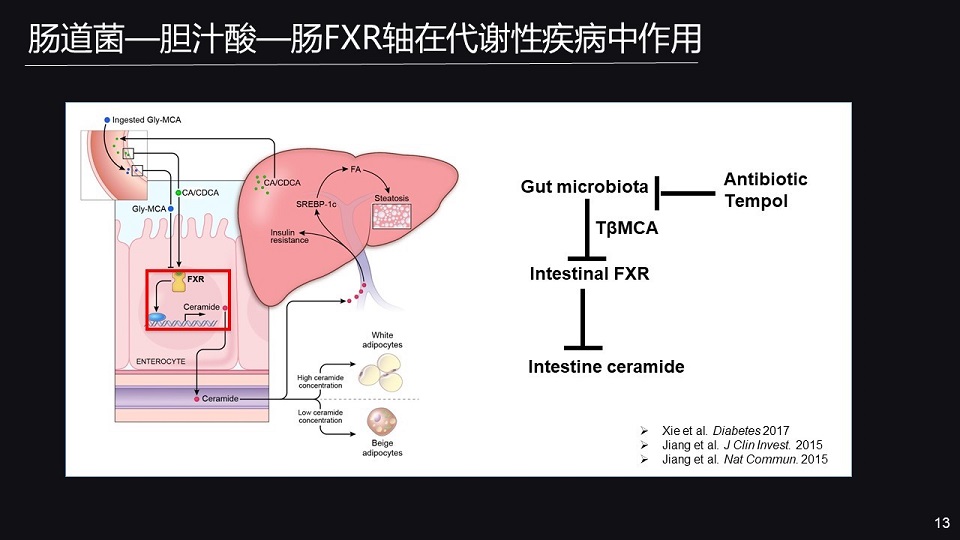
那究竟是什么样的机制介导的FXR对代谢的调节作用呢?
我们通过代谢组学发现,肠FXR能够调控鞘酯神经酰胺的代谢,肠FXR被激活之后,它能够促进神经酰胺的释放。
神经酰胺能进一步引起肝脏的胰岛素抵抗与脂质的生成,同时能够抑制白色脂肪棕色化。
那在最近的几个临床的RCT(随机对照试验)研究中,就发现鞘酯神经酰胺是代谢性疾病的一个独立的危险因素,它能够明显的促进胰岛素的抵抗与心血管的不良事件。
那我们的结果呢,发现抑制肠FXR信号,可以通过减少神经酰胺的释放,发挥抗肥胖、糖尿病和脂肪肝的作用。
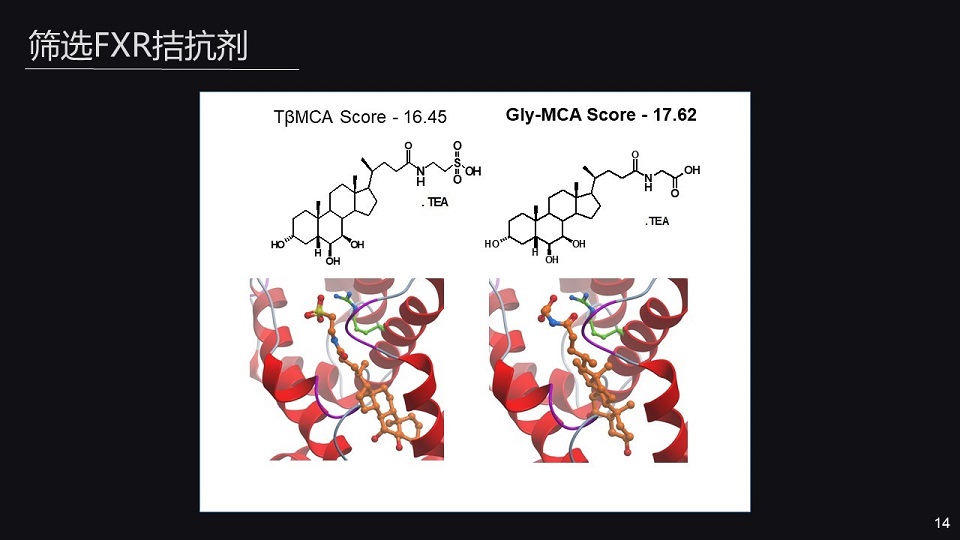
既然肠FXR是一个非常重要的代谢性疾病的干预的药靶,那我们就希望对肠FXR的拮抗剂进行一个筛选。
那么我们已经发现,胆汁酸T-βMCA实际上是FXR的一个内源性拮抗剂。但T-βMCA能够被肠道菌水解,所以说影响了它对糖尿病的治疗效果。
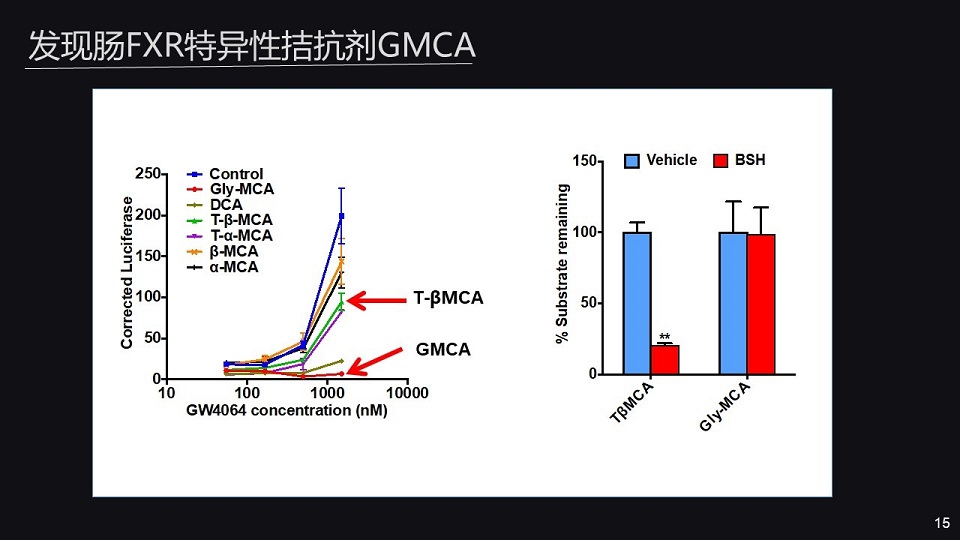
那我们就希望找到新型的FXR的拮抗剂,通过筛选,我们找到了GMCA。那GMCA与T-βMCA相比呢,有更高的拮抗作用,那更为重要的是它能够抵抗肠道菌的水解作用。
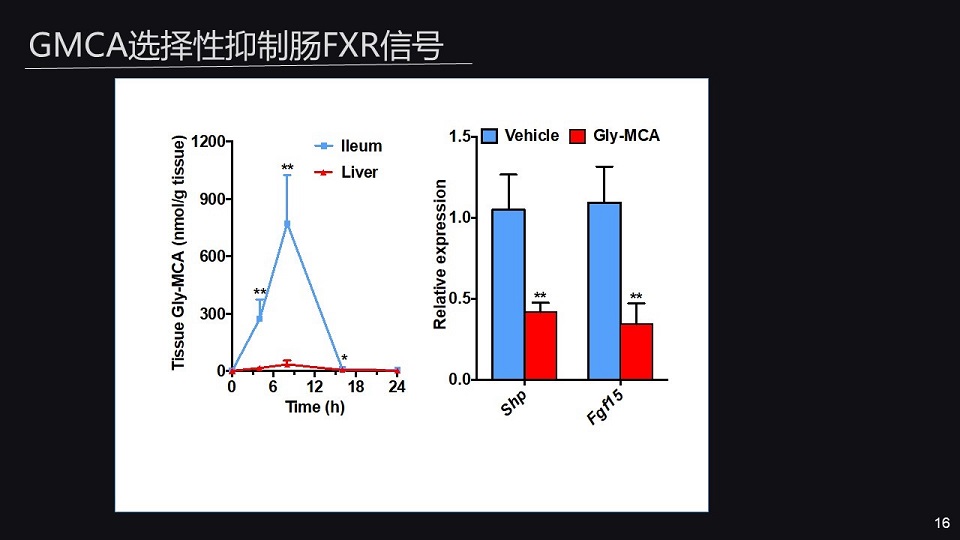
进一步药代动力学的研究发现,给予GMCA之后,它主要停留在肠道而很少吸收入血,特异的抑制肠FXR但不影响肝FXR,这就能有效的避免其潜在的副作用。
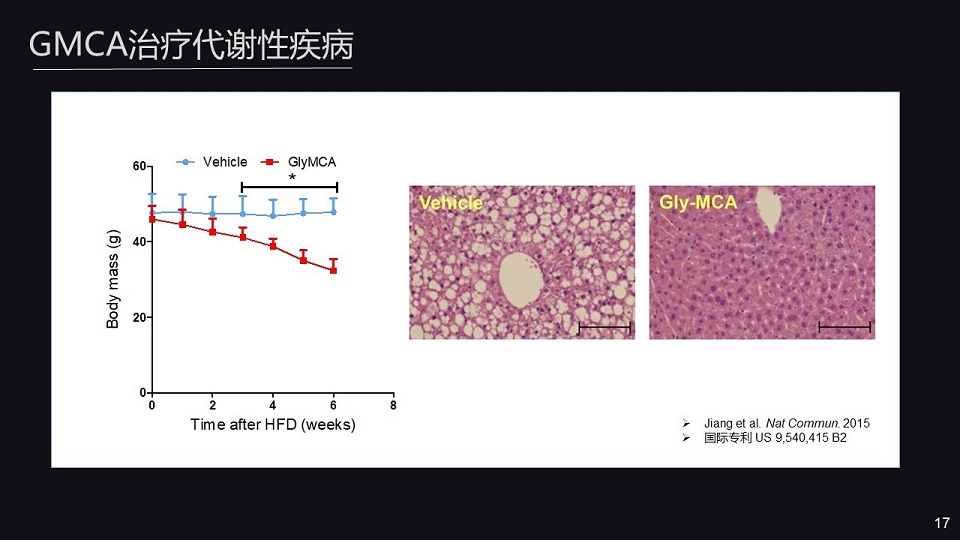
我们给予高脂饮食以及db/db敲除的糖尿病小鼠GMCA处理。
我们发现给予GMCA治疗之后,小鼠的体重明显的减轻,血糖明显的降低,胰岛素的敏感性增加,脂肪肝的程度也减轻了。
那么在人体中,是否有药物也能够通过靶向肠道菌-胆汁酸-肠FXR信号,发挥治疗糖尿病的作用呢?
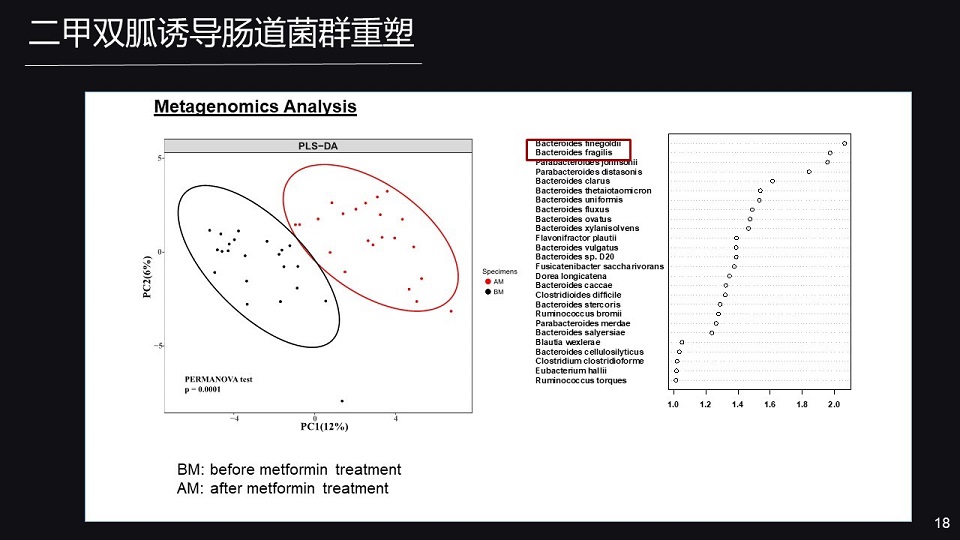
二甲双胍是目前临床治疗II 型糖尿病的首选药物,但二甲双胍的作用靶点比较多。
最早人们发现二甲双胍主要作用的器官是在肝脏,随后人们的研究发现,在其他组织,如肠道,也是二甲双胍的一个重要靶点。但肠道在二甲双胍发挥降糖作用当中的作用呢,目前尚不清楚。
那我们系统的分析了初诊II 型糖尿病患者,在给予二甲双胍治疗之后肠道菌群的变化。
短期给予二甲双胍能够明显的引起肠道菌群重塑,主要表现于脆弱拟杆菌的丰度显著的被抑制。
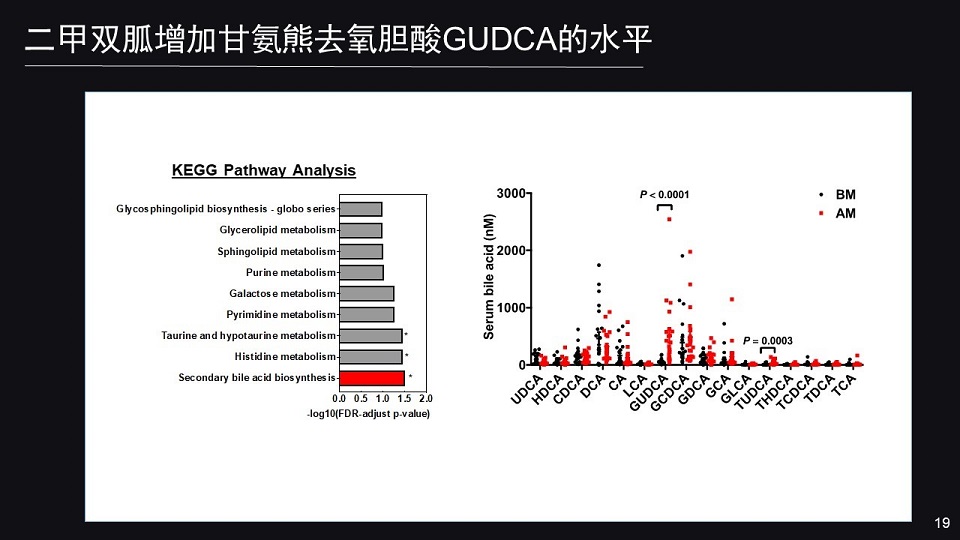
KEGG通路分析研究结果提示,二甲双胍能明显的影响次级胆汁酸的代谢。我们进一步运用代谢组学分析,发现给予二甲双胍之后,甘氨熊去氧胆酸(GUDCA)的水平显著增加。
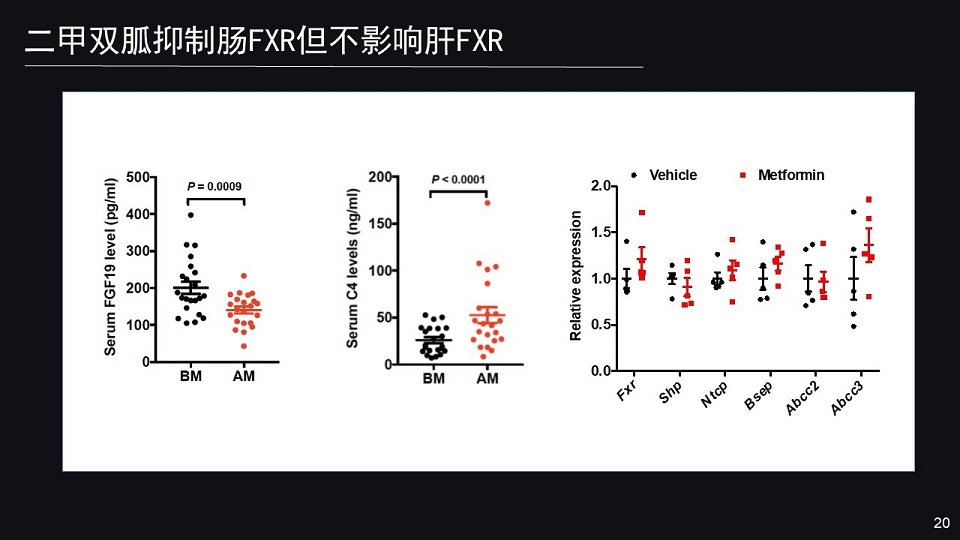
同时我们发现,血浆FGF19的水平明显的降低,FGF19是肠FXR的一个靶基因;同时血浆当中的C4(7-羟基-4-胆甾烯-3-酮 C4)的水平明显的增加。
这些都反映肠FXR在二甲双胍干预之后,明显的被抑制,但是肝FXR的信号却没有显著的改变。
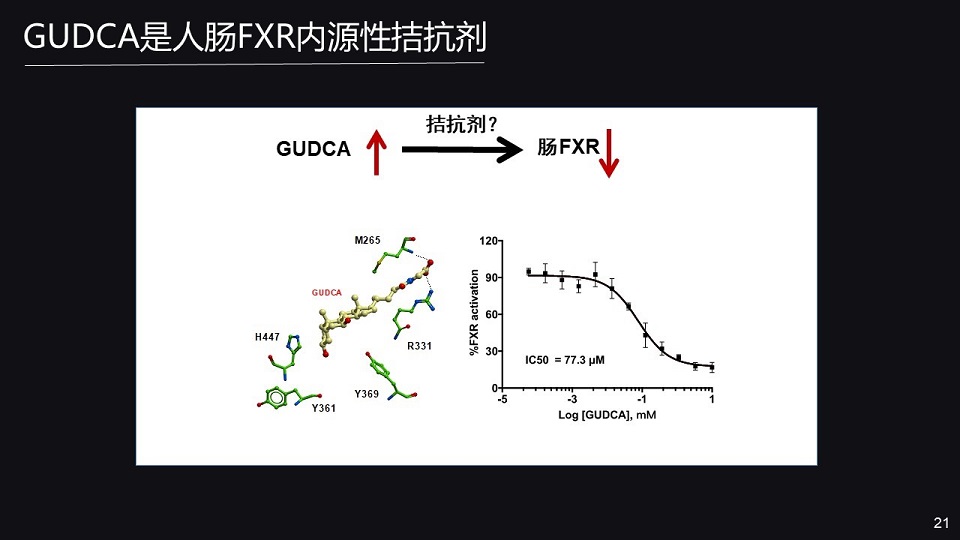
我们的研究结果发现,给予二甲双胍之后,胆汁酸GUDCA的水平显著增加;而对应的,肠FXR的信号被抑制。这就提示GUDCA可能是肠FXR拮抗剂。
我们通过生物信息学及其其他的生物学手段,证实了我们的假说, GUDCA确实是人肠FXR内源性拮抗剂。
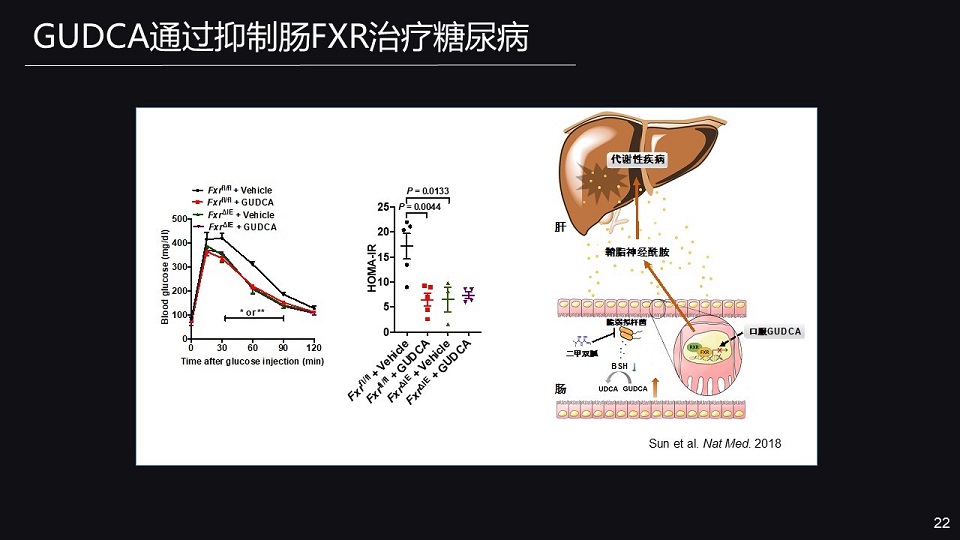
我们也给予糖尿病小鼠胆汁酸GUDCA的干预,我们发现给予GUDCA治疗之后,它的体重明显减轻,血糖明显改善,胰岛素敏感性也增加了,这能够有效的治疗糖尿病。
并且GUDCA的这种作用,还特异的依赖于抑制肠FXR信号。
总之,我们的研究结果提示,二甲双胍通过靶向肠道脆弱拟杆菌、胆汁酸GUDCA以及肠FXR这个轴发挥其降糖作用,胆汁酸GUDCA是肠FXR内源性拮抗剂。我们提出了干预代谢性疾病的新靶标,即抑制肠FXR信号通路。

胆汁酸的信号通路在代谢性疾病当中发挥一个极其重要的作用,是重要的药物干预靶点。那以下列出来的,就是针对胆汁酸的几种药物的研发情况。
首先是CDCA及其衍生物,其中备受人们瞩目的是奥贝胆酸。
在今年(2019年)刚刚结束的,针对非酒精性脂肪性肝炎(NASH)的三期临床结果显示,奥贝胆酸能够明显的减轻NASH患者的肝脏的纤维化。
很有可能,奥贝胆酸将成为首个被批准的用于NASH这一适应症的药物。那三年前,奥贝胆酸也被批准了用于原发性胆汁性胆管炎(PBC)的治疗。
另外一种CDCA衍生物INT-767,主要的靶点是激活肝脏的FXR与TGR5这两种信号通路。它目前在临床一期,也是针对原发性的胆汁性的胆管炎。
那另外一种衍生物INT-777,主要是激活TGR5。它目前处于临床前,它的一个适应症,就是NASH。
第二类是UDCA及其衍生物。
那谈到UDCA,其实在临床上是一个老药。它能够主要用于胆汁淤积类的肝病,比如说前面提到的原发性的胆汁性的胆管炎,还有它能够显著的改善肝功能。
其中一个衍生物TUDCA,已经被批准用于胆结石的治疗;另外一种衍生物NUDCA,目前是在临床二期,是针对原发性的胆汁性的胆管炎的治疗。
那第三类就是胆汁酸的螯合剂,比如消胆胺;还有另外一类,与它功能相似,就是胆汁酸转运体ASBT的抑制剂。
它们共同的作用的靶点都是通过抑制胆汁酸,进一步能够抑制肠FXR信号,对于II 型糖尿病具有治疗的作用。

那最后,感谢我的团队还有我的合作者,谢谢大家!


