编者按:
多项研究表明,检查点抑制剂与微生物组疗法的组合,可以增强患者对免疫疗法的应答。当前,已经有许多微生物组初创公司开始开展相关的临床试验。
那么,有哪些微生物组公司正在行动呢?又有哪些类型的微生物组疗法呢?
今天,我们共同关注微生物组疗法与检查点抑制剂,特别编译发表在 Nature Biotechnology 杂志上题为“Fecal microbiota potentiate checkpoint inhibitors, unleash microbiome startups”的文章。希望本文能够为相关的产业人士和诸位读者带来一些启发与帮助。
发表于 Science 杂志上的两篇论文表明,粪菌移植(FMT)可以提高免疫检查点抑制剂的抗癌效果,这为 FMT 与免疫疗法的联合作用,提供了第一个临床证据。
为此,至少有 8 家微生物组公司已经启动了首次人体试验,将微生物组制剂与获批的免疫疗法联合(表1),以满足日益增长的需要——增加检查点抑制剂应答患者的比例。
“免疫检查点抑制剂是个好东西,”德国默克公司全球开发主管 Danny Bar Zohar 说,“但问题是绝大多数人对它不应答。”这背后可能蕴含着各种机制作用,可能与患者基因组学或蛋白质组学有关,但新的数据表明,肠道微生物组在调节患者的应答中,起着重要的作用。
特拉维夫大学的免疫肿瘤学家、其中一篇 Science 论文的共同作者 Gal Markel 说,这两项早期临床研究,可以相互验证。“两个独立的研究团队,研究出了完全相同的结果,这是非常有力的证据。”
这两项研究,都把对抗程序性细胞死亡蛋白 1(PD-1)治疗有应答的转移性黑色素瘤患者的肠道菌群,移植到了对这些疗法没有应答或已停止应答的患者身上。
在第一项研究的 10 名患者中,5 名患者接受了同一位供体的 FMT 治疗,其中 3 名出现显著应答,其中 1 名完全应答。在接受另一位供体 FMT 治疗的 5 名患者中,有 2 名有应答,2 名病情稳定。
第二项研究,由匹兹堡大学和美国国家癌症研究所(NCI)的研究人员领导,是一项两阶段的单中心研究,即在 PD-1 抑制剂治疗无效的黑色素瘤患者中,同时使用检查点抑制剂和 FMT 治疗。
他们报道,16 名接受 FMT 治疗的患者中,有 3 名出现显著应答,包括 1 名完全应答,还有 3 名患者病情长期稳定。
不过,研究之间的微小差异,使得研究人员很难得出具体的结论。第一项研究使用的检查点抑制剂,是百时美施贵宝(BMS)公司的 Opdivo(nivolumab)——一种完全人源化的 IgG4 单克隆抗体(mAb),作用靶点是 PD-1 受体。在给患者进行 FMT 治疗(通过结肠镜和口服胶囊)之前,研究人员用抗生素清除了他们已有的肠道菌群。
而第二项研究使用的检查点抑制剂,是美国默克公司的 Keytruda(pembrolizumab)——一种完全人源化的 Ig4κ 单克隆抗体,靶向 PD-1 受体配体 1(PD-L1)和 PD-L2。
在第二项研究中,研究人员避免使用抗生素,因为大量的证据表明,抗菌药物会对癌症患者的生存,产生负面影响。并且用于 FMT 治疗的肠道菌群,来自于同一个供体。
尽管有以上的不同,但两项研究之间,依然存在相似之处。匹兹堡大学医学中心希尔曼癌症中心的研究人员、第二篇论文的共同作者 Hassane Zarour 指出,在最初抗 PD-1 治疗无效的患者中,通常只有不到 10%的患者,可以转变为应答者。
而在他的试验中,44%的患者至少病情稳定,而在另一项研究中,有一半的患者病情稳定。“虽然没有统计证据,但显然比预期的要多得多。”
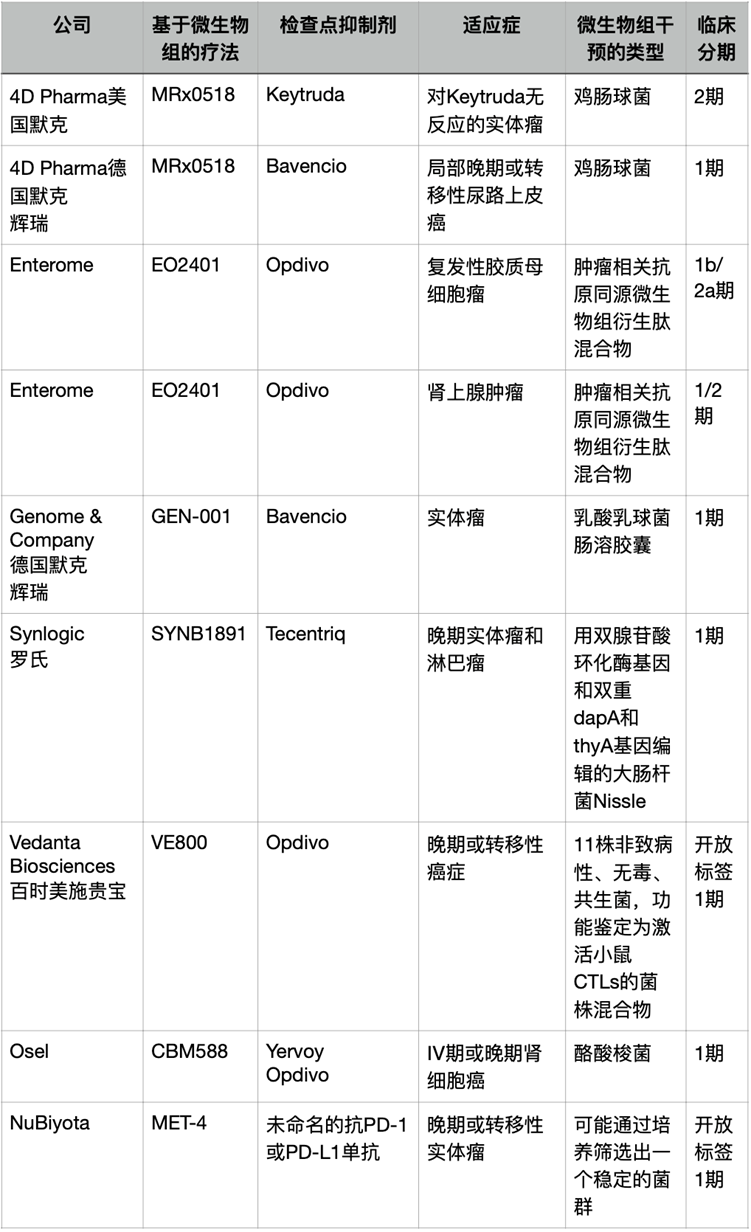 表1 临床联合应用微生物组或微生物组衍生产品-检查点抑制剂的代表性公司
表1 临床联合应用微生物组或微生物组衍生产品-检查点抑制剂的代表性公司
在第一个检查点抑制剂 Keytruda 于 2015 年获得批准后不久,肠道菌群可能影响癌症患者对免疫治疗的应答的观点就被提出了。
当时,古斯塔夫-鲁西研究所的免疫学家和肿瘤学家 Laurence Zitvogel,通过小鼠模型发现,共生细菌脆弱类杆菌,与细胞毒性 T 淋巴细胞(CTL)抗原 4(CTLA-4)阻断抗体的抗肿瘤免疫反应存在关联,不仅如此肠道中是否存在该菌株,与 Yervoy(ipilimumab)的临床应答存在关联。而 Yervoy 是一种用于黑色素瘤患者的 IgG1κ 单抗,靶向 CTLA-4。
随后,由芝加哥大学肿瘤学家 Thomas Gajewski 领导的研究团队发现,一种独特的双歧杆菌,能够提高抗 PD-L1 药物在小鼠黑色素瘤模型中的疗效。
另一篇具有里程碑意义的论文发表于 2018 年,由美国德州大学 MD 安德森癌症中心的肿瘤学家 Jennifer Wargo 领导的研究团队发现——瘤胃球菌科细菌是人类抗 PD-1 疗法临床应答的关键。
Gajewski 的研究促成了他与 Evelo Therapeutics 公司的合作,该公司于 2019 年启动了最早的微生物组-检查点抑制剂联合临床试验之一,对单株动物乳双歧杆菌进行了测试,既作为单药,也与美国默克公司的 Keytruda 联合给药。
Evelo Therapeutics 公司正在开发单一菌株的和细胞外囊泡两种疗法。2020 年 12 月,Evelo Therapeutics 公司向美国默克公司提交了中期试验数据,显示动物乳双歧杆菌-Keytruda 联合疗法是安全的,并且耐受性良好。
即便如此,该公司还是放弃了该计划,转而支持 EDP1908 候选药物。这是一种来源于未发表的颤螺旋菌科菌株的细胞外囊泡疗法,在肿瘤微环境中,该菌株表现出对效应淋巴细胞群的有效激活作用。
与FMT相比,单一菌株具有一些实际优势:它们更易于表征和制造。因此,几家药品开发商都采取了这种策略。例如,位于英国利兹的 4D Pharma 公司,正在进行 MRx0518 疗法与 Keytruda 联合应用的 1/2 期试验,MRx0518 疗法是一种口服的鸡肠球菌菌株,具有 Toll 样受体(TLR)-5 激动剂的功能。
2020 年公布的中期数据显示,12 名肾细胞癌和非小细胞肺癌患者对该疗法的耐受性良好,而这些患者此前对免疫检查点抑制剂不应答。4D Pharma 公司的首席科学官 Alex Stevenson 说,与最近发表的 FMT 研究结果相比,“我们在肿瘤治疗后,也看到了非常相似的生物学现象。”
美国默克公司和 4D Pharma 公司计划将研究对象扩大到 120 名肾细胞癌、非小细胞肺癌或其他对免疫治疗无应答的实体瘤患者。
2021 年 2 月,4D Pharma 公司宣布与另外两家公司——德国默克公司和辉瑞公司合作,将 MRx0518 疗法与后者的 Bavencio(avelumab,一种靶向 PD-L1 的人类 IgG1λ 单克隆抗体)进行联合治疗,开展 1 期试验。
Bavencio 是唯一一种免疫疗法,被批准用于局部晚期或转移性尿路上皮癌,该试验将测试上述联合疗法,能否作为该类癌症患者的一线维持疗法。
韩国微生物组学机构 Genome & Company 公司,也将 Bavencio 与自己的 GEN-001 疗法联合起来进行试验,GEN-001 是一种肠溶胶囊,至少含有 1×1011 CFU 的乳酸乳球菌(对免疫疗法应答肺癌患者的微生物组进行 16S 核糖体 RNA 分析鉴定得到)。
2020 年,在 1/1b 期试验中,研究人员给第一批实体肿瘤患者服用了上述联合药物。
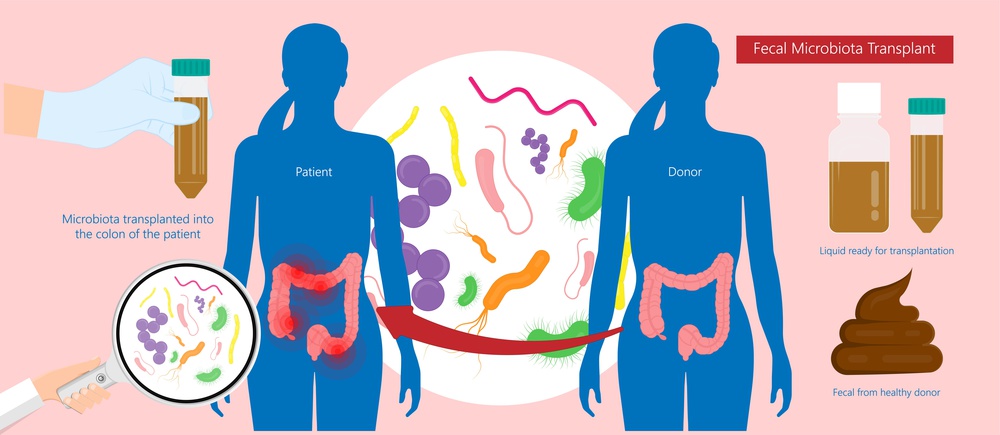
然而,与使用单一的微生物菌株,或利用特定菌株组成的活体生物药(LBPs)相比,利用 FMT 将整个微生物组移植给受体来干预疾病的临床记录历史更悠久。
FMT 通常是安全的;它们通过结肠镜或口服制剂给药,并作为其他疾病领域(如复发性艰难梭菌感染)标准护理的一部分,定期进行。
迄今为止,FDA 关于 FMT 研发的最新指导,是一份 2016 年的文件,专门用于复发性艰难梭菌感染。
2019 年,当两名免疫功能低下的患者因 FMT 出现抗生素耐药肠侵袭性大肠杆菌感染时,FDA 勒令 FMT 研发人员对 FMT 产品中的多重耐药菌,进行额外的筛查。
2020 年 4 月,FDA 再次强调,要解决 FMT 中 SARS-CoV-2 的感染风险。由于 FMT 也被开发用于癌症免疫治疗,所以上述这些微生物组产品的发展,可能会遵循类似的轨迹。
据 NCI 癌症免疫学综合实验室主任 Giorgio Trinchieri 所说:“他们不能像调节任何普通生物制剂那样,严格地调节 FMT 的成分。”他说,并且,产品成分的差异性,以及从 FMT 供体样本中去除潜在病原体所需的额外筛查程序,可能使这些产品的研发更具挑战性。
Trinchieri 发表了一篇论文,该论文论述了 FMT 治疗时应避免抗生素的使用。他还指出,定植问题增加了 FMT 的复杂性。FMT 治疗将一个微生物组添加到原有的微生物组中,这将会创造一个新的生态。
“不论你要移植的微生物有 1 种、10 种或 20 种,你都必须确保,这些微生物可以在患者体内定植,并且你最终得到的变化是稳定和有利的。”
为了寻找更简单、更明确的产品,有些微生物组公司以 FMT 作为起点,来发现特定的微生物菌株,并将其整合到 LBP 中。Ella Therapeutics 公司的科学联合创始人和首席医疗官 Markel,就是采用了这种方法——他们通过研究检查点抑制剂应答者的肠道微生物组,来开发产品。
与此同时,英国剑桥的 Microbiotica 公司,筛选出了那些确实对免疫疗法有应答的患者,并已鉴定出了 9 株能预测患者应答的菌株。而这些微生物菌株特征,可作为其他公司预测免疫疗法应答的生物标志物。
这 9 株菌株的混合物,也可以作为 LBP 的基础进行研发,混合物中的不同菌株,可以为肿瘤免疫的不同环节添砖加瓦,例如树突状细胞的成熟、白细胞介素-12 促进 CTL 启动、通过 TLR-3 激活 CTL、辅助性 T 细胞 1(TH1)定向应答辅助 CTL 杀死肿瘤细胞。
为了避免 FMT 的不可预测性,Vedanta Biosciences 公司也在研发确定的细菌混合物产品,以在肠道中实现良好的定植。该公司的先导药物 VE800(一种 11 种菌株的组合),正与 BMS 公司的 Opdivo 疗法联合应用,进行 1 期试验。在与 Vedanta Biosciences 公司共同进行这项试验的同时,BMS 公司还对其进行了股权投资。
“利用一个确定、已知的产品,我们可以塑造患者的应答情况,取得更良好的微生物定植。”Vedanta Biosciences 公司的首席执行官 Bernat Olle 如是说。
并非所有确定的微生物制剂,都能取得成功。2021 年 4 月初,Seres Therapeutics 公司宣布,它将停止对于 SER-401(一种确定菌株的混合物)的1期试验,该试验原计划将 SER-401 与 BMS 公司的 Opdivo 联合应用于转移性黑色素瘤。
尽管 Seres Therapeutics 公司宣称 SER-401 很安全,并且耐受性良好,但依然决定“暂缓 SER-401 的进一步研究”,并继续实施其他项目。
与其依赖于确定的未修饰菌株混合物,另一种研发 LBP 的方法,是利用分子工程进行修饰。Synlogic 公司的基因工程大肠杆菌 Nissle 菌株(SYN1891),就被设计成可以直接注射到肿瘤组织中,该方法类似于 130 多年前 William Bradley Coley 首创的方法。
SYNB1891 菌株,含有单核细胞增生李斯特菌的二腺苷酸环化酶基因和其他两个基因——dapA(编码二氢吡啶二羧酸合成酶,参与赖氨酸的生物合成)和 thyA(编码胸苷酸合成酶,参与胸苷酸的生物合成)——它们的表达受启动子的控制,该启动子仅在缺氧的肿瘤微环境中启动。
这样的条件选择机制,会迫使 SYN1891 菌株在恶性组织中复制增殖。当然,这种在人体中不能自然存在的基因工程 LBP,很可能会受到 FDA 最严格的审查。
Synologic 公司的首席医疗官 Richard Riese 认为,异源二腺苷酸环化酶,可增加环二核苷酸 2′,3′鸟苷酸-腺苷酸(cGAMP)的水平,而 cGAMP 是 STING(干扰素基因刺激蛋白)蛋白通路中的信号分子,会被抗原呈递细胞优先摄取,刺激 CD4+ 和 CD8+ T 细胞的应答。
Riese 说,其他研究人员已经表明,胃肠道可用于抗肿瘤免疫,但与肿瘤部位注射的效果相比,这种作用是间接的;迄今为止,还没有人能够通过成功的药物或 LBP,挖掘出肠道的抗肿瘤机制。
Synologic 公司正将 SYNB1891 与靶向 PD-L1 的 Tecentriq(Atozolizumab)疗法联合起来,作为实体瘤和淋巴瘤的单一治疗进行 1 期试验,Atozolizumab 是 Roche 公司研发的一种 Fc 工程化、人源化、非糖基化的 IgG1κ 单克隆抗体,靶向 PD-L1。
最后一种方法,是将重心放在微生物组产生的肽上。总部位于巴黎和剑桥的 Enterome 公司,正在与 BMS 公司合作,检测微生物组来源的肽抗原与 Opdivo 疗法以及 EO2401 疗法联合应用的效果,该研究是一个两阶段的 1/2 期试验,Enterome 公司称,这种肽抗原可激发患者对肿瘤的免疫应答。
目前,这些生物公司和研究人员研究出来的结果,仍然少于他们提出的问题。NCI 的 Trinchieri 说,目前尚不清楚,到底是哪些微生物,在哪些患者的哪些肿瘤中,对哪些检查点抑制剂的应答,起到关键的作用。
他说:“对 CTLA-4 有用的免疫疗法,不一定对 PD-1 有用。”例如,类杆菌似乎对抗 CTLA-4 疗法有积极作用,但对抗 PD-1 疗法有消极作用。“目前,我不会说你已经可以从一种免疫检查点抑制剂或一种肿瘤类型,推断出另一种的情况。”
即使是同样针对抗 PD-1 疗法,五项已发表的临床微生物组学研究,发现与应答有关的微生物也不相同:Arthur Frankel 于 2017 年发表的论文——粪拟杆菌;Zitvogel 于 2018 年发表的论文——Akkermansia muciniphila;Gajewski 于 2018 年发表的论文——长双歧杆菌;Wargo 于 2018 年发表的论文,Faecalibacterium 和普拉梭菌;Markel 于 2021 年发表的论文——肠球菌科、肠球菌和链球菌。
原文链接:https://www.nature.com/articles/d41587-021-00002-w
作者|Mark Zipkin
编译|Jessica
审校|617
编辑|笑咲


