
编者按:
近10年来,中国乃至亚太地区,溃疡性结肠炎(UC)发病人数呈现增长状态,其中中国UC患病人数增长了数十倍。那么,当前UC有哪些治疗方式?有哪些正在研发的新疗法?未来市场规模如何?
今天,我们特别编译 Nature Reviews Drug Discovery 杂志发表的关于 UC 市场的文章。希望本文能够为相关的产业人士和诸位读者带来一些启发和帮助。
溃疡性结肠炎(UC)是一种炎症性肠病(IBD),该疾病会影响结肠和直肠的粘膜以及粘膜下层,有时也会影响到回肠末端的一小段。严重UC的特征包括发烧,C 反应蛋白和血红蛋白水平异常,以及其他肠道炎症迹象。UC 的并发症可能是局部的,比如痔疮、肛周脓肿或肛裂,也可能出现肠外表现。据估计,UC 的发病率为每 10 万人 7 到 246 例。
与传统疗法相比,近年来兴起的生物疗法,如肿瘤坏死因子(TNF)拮抗剂和抗 α4β7 整合素抗体维得利珠单抗,对 UC 具有更好的控制效果。不过目前,有许多新兴疗法即将上市或处于开发后期阶段,并可能比现有疗法具有更好的疗效。
轻中度 UC 患者的一线治疗包括口服氨基水杨酸盐和控释布地奈德。急性 UC 患者通常使用全身性皮质类固醇。巯嘌呤或硫唑嘌呤可替代 TNF 抑制剂或与其联合使用,以维持 UC 的缓解,同时也可用于氨基水杨酸盐无效或长期需要使用全身性皮质类固醇的患者。肠外注射环孢菌素也可有效治疗皮质类固醇难治的严重 UC,并可延迟甚至消除手术需求。
对于中重度UC患者或皮质类固醇依赖的患者,肠外治疗方案通常涉及 TNF 抑制剂,包括英夫利昔单抗(Remicade,杨森制药)、阿达木单抗(Humira,艾伯维)和戈利木单抗(Simponi,杨森制药)。
整合素阻断治疗也可用于治疗中重度 UC 患者。维得利珠单抗(Entyvio,武田制药)是一种人源化单克隆抗体(mAb),能与 α4β7 整合素结合,从而阻断白细胞迁移至肠道。维得利珠单抗作为二线肠外治疗,用于因副作用、疗效缺失或丧失反应而无法使用抗 TNF 药物进行治疗的中重度 UC 患者;作为一线治疗,用于采用抗 TNF 治疗可能会产生更大风险的患者。
其他治疗中重度 UC 患者的策略包括 JAK 抑制剂,以及可以特异识别 IL-12 和 IL-23 共有亚基 p40 的抗体。
乌司奴单抗(Stelara,杨森制药)是一种通过与 p40 结合的单克隆抗体,可阻断细胞信号传导、细胞因子产生和免疫成分基因表达。
托法替尼 (Xeljanz,辉瑞) 是一种具有口服活性的JAK家族激酶的非选择性抑制剂。它会影响多种可调节 B、T 淋巴细胞的白细胞介素的产生,这些白介素与粘膜炎症有关。
然而,一项研究表明,与TNF抑制剂治疗相比,托法替尼更容易造成类风湿性关节炎老年患者发生严重不良事件,因此托法替尼和JAK抑制剂的安全性受到了质疑。
基于此,美国 FDA 正在审查目前已批准的用于炎症疾病治疗的 JAK 抑制剂的标签。目前,已获批准的 JAK 抑制剂的标签上已经添加了严重感染、恶性肿瘤和血栓形成的黑框警告信息。
奥扎莫德(Zeposia,百时美施贵宝)是一种1-磷酸鞘氨醇(S1P)受体调节剂,可阻断淋巴细胞从淋巴结中流出的能力,从而减少慢性炎症部位的淋巴细胞数量。此前该药物已经被批准用于治疗多发性硬化症,并在 2021 年 5 月被 FDA 批准用于治疗中重度 UC。
在 True North III 期临床试验中,中重度 UC 患者在使用为期 10 周的奥扎莫德后,临床缓解发生具有统计学意义的改善(18%,安慰剂组为6%)。此外,第 52 周时,使用奥扎莫德维持治疗的患者达到临床缓解的比例(37%)明显高于安慰剂组(19%)。
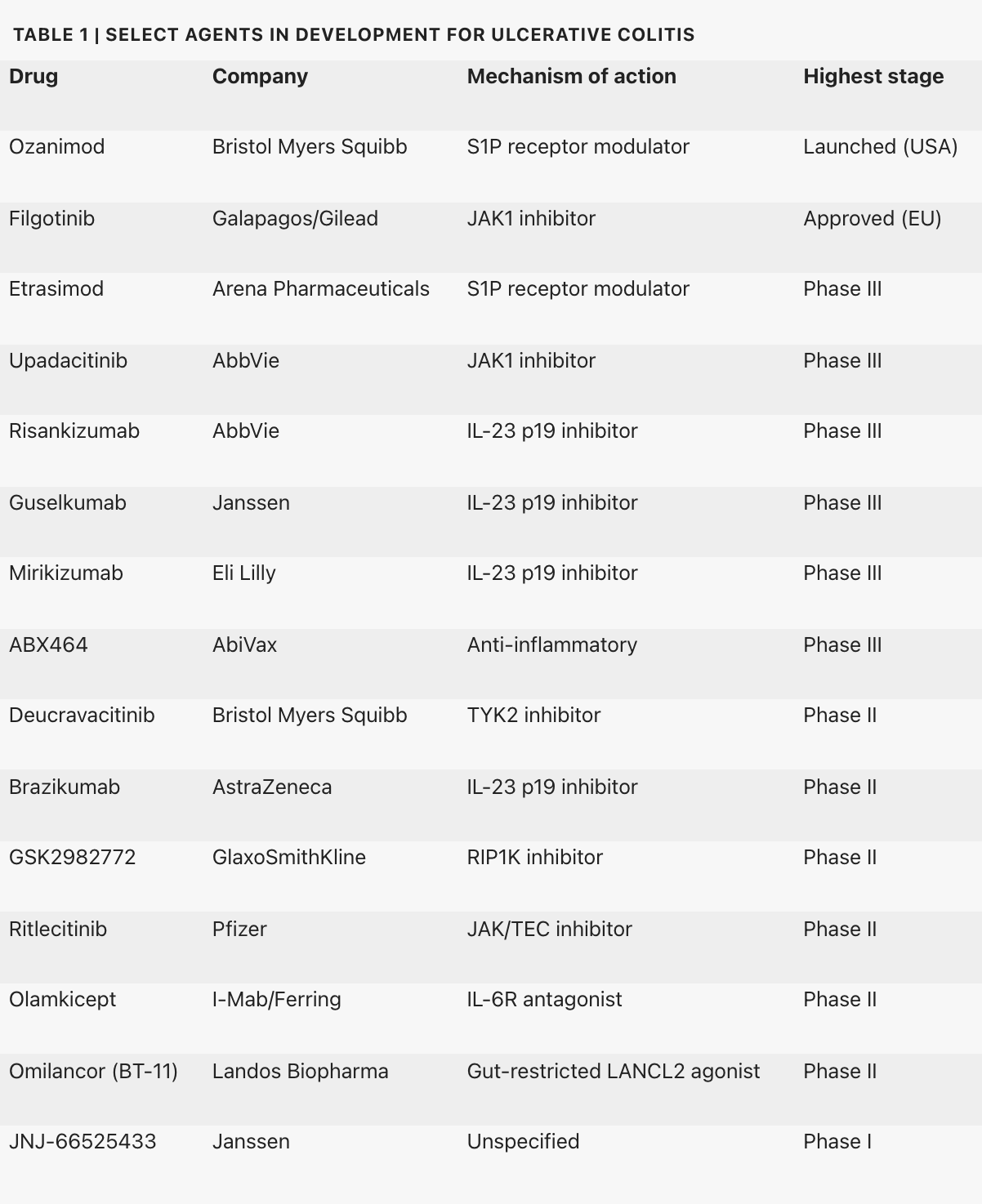
表1. 正在开发中或即将上市的UC新疗法。
UC 的新兴疗法往往针对中重度活动期UC患者,并且主要是口服小分子药物和注射生物制剂。这些新疗法往往采用了一种新的机制,或比目前开发的治疗策略具有更好的选择性(表1)。
2021 年 11 月份,新型选择性 JAK 抑制剂非戈替尼((Jyseleca;Galapagos/吉利德),在欧盟被批准用于治疗中重度 UC。另一种用于治疗中重度 UC 的 JAK 抑制剂乌帕替尼(Rinvoq;艾伯维)也在开发中。相比于 JAK2 和 JAK3,这两种药物对 JAK1 的选择性更强,因此只抑制某些信号通路。它们有望在不降低疗效的情况下,降低剂量相关的毒性。
在 III 期 U-ACCOMPLISH 和 U-ACHIEVE 试验中,第 8 周时,接受乌帕替尼治疗的患者分别有 33% 和 26% 达到了临床缓解,而安慰剂组只有 4% 和 5% 的患者达到了临床缓解。此外,与接受安慰剂治疗的患者相比,有更多接受乌帕替尼治疗的患者在第52周达到临床缓解(15 毫克剂量和 30 毫克剂量的患者临床缓解率分别为 42% 和 52%,而安慰剂组仅为 12%)。
Etrasimod (Arena Pharmaceuticals)是一种每日一次用于治疗中重度 UC 的口服选择性 S1P 受体调节剂,目前正进行 III 期试验(ELEVATE UC 52 和 ELEVATE UC 12)。Etrasimod 对 S1PR1(S1P 受体 1)、S1PR4 和 S1PR5 具有选择性,而且半衰期短,因此预计这种疗法的脱靶效应比奥扎莫德要低。
另外一种正在开发用于治疗UC的口服活性小分子是 deucravacitinib (百时美施贵宝),它是一种酪氨酸激酶 2(TYK2,JAK 家族激酶的成员之一)选择性变构抑制剂。Deucravacitinib 的作用机制与其他 JAK 抑制剂不同,它通过与调节域结合而非与活性位点结合来抑制 TYK2。
虽然 TYK2 变构抑制剂的选择性更强,并有可能避免大部分与活性部位直接结合的 JAK 抑制剂的副作用,但在 II 期 LATTICE-UC 试验中,与安慰剂组相比,deucravacitinib 在第 12 周的主要终点临床缓解以及关键的次要终点方面,未能显示出优势。针对 UC 的第二项 II 期试验正在进行中。
另外两种 JAK 家族抑制剂,辉瑞公司的 ritlecitinib(PF-06651600)和 brepocitinib(PF-06700841)近期也完成了 II 期开发。ritlecitinib 是 JAK3/TEC 的不可逆抑制剂,brepocitinib 是 TYK2/JAK1 抑制剂。
在 II 期 VIBRATO 研究中,接受 ritlecitinib(70 毫克剂量或 200 毫克剂量)治疗的患者在第八周达到临床缓解的人数明显多于接受安慰剂治疗的患者(临床缓解率分别为 34%、29% 和 0%)。
其他的正开发用于 UC 治疗的口服小分子药物包括葛兰素史克公司的 GSK2982772,它是一种受体相互作用丝氨酸/苏氨酸蛋白激酶 1(RIP1K)抑制剂。
四种特异性靶向 IL-23 的药物而非与 IL-12 共有亚基的药物也正在被开发用于治疗 UC。这些单克隆抗体选择性地结合到 IL-23 的 p19 亚单位,从而抑制其与 IL-23 受体的相互作用以及由此产生的下游信号:
1.瑞莎珠单抗(Skyrizi,艾伯维)已经被批准用于治疗中重度斑块状银屑病,现在它正进行中重度 UC 的 III 期试验。
2.mirikizumab(LY3074828,礼来)也处于针对中重度 UC 的 III 期开发阶段。
3.被批准用于治疗成人中重度斑块状银屑病以及治疗成人活动性银屑病关节炎的古塞库单抗(Tremfya,杨森)正在进行治疗中重度 UC 的 III 期试验。此外,杨森公司正在开展一项II期研究,评估古塞库单抗与戈利木单抗联合治疗 UC 的有效性和安全性。
4.阿斯利康的 brazikumab (MEDI2070),正在进行中重度活动期 UC 的 II 期试验。
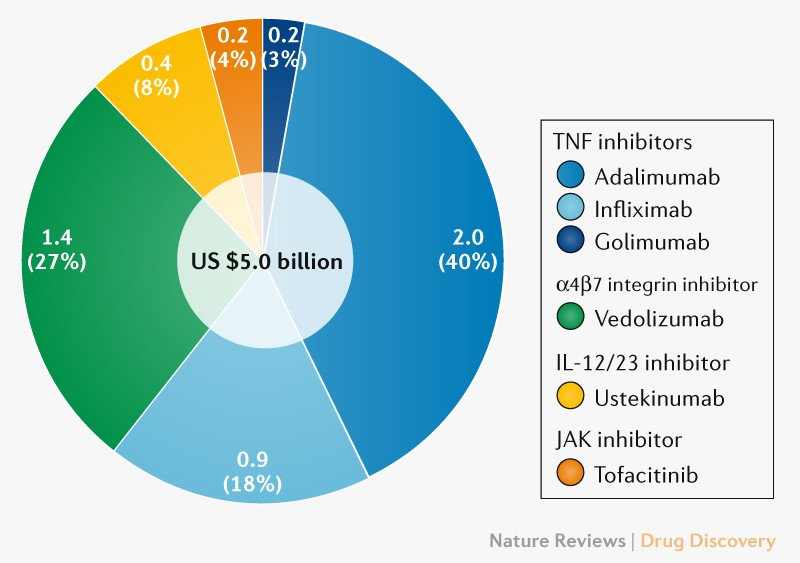
图1. 2020年美国溃疡性结肠炎的市场。
2020年,全球 UC 药物市值约 75 亿美元(约合 476 亿人民币),占整个免疫学市场的 10%。美国仍然是 UC 治疗的主要市场,占总销售额的 65%(图1)。在过去的 4 年里,UC市场规模以 10% 的年复合增长率(CAGR)增长,主要是由诊断率的提高、新兴疗法的引入和生物制剂在中重度患者中的使用增加所驱动的。
阿达木单抗(在美国独占,Humira)以 40% 的市场份额在美国 UC 市场上占主导地位,其次是维得利珠单抗(在美国仅为 Entyvio;27%),然后是英夫利昔单抗(Remicade 及其生物仿制药;18%)。
尽管市场分析会受到这些药物在其他适应症上的使用的干扰,但 2020 年以后全球 UC 市场前景大好,预计复合年增长率为 5~7%。这种增长主要是由几种新兴疗法(主要是 IL-23 和 JAK 抑制剂)的引入推动的。按照目前的增长率,预计 2026 年,UC 全球市场规模将达到 110~120 亿美元。
然而,新兴疗法将受到生物仿制药的挑战,因为包括 Humira、Entyvio 和 Remicade 在内的主要品牌将从 2023 年起失去在美国的“排他性”。
原文链接:
https://www.nature.com/articles/d41573-021-00194-5
作者|Rami Al-Horani , Eleonora Spanudakis 和 Bashar Hamad
翻译|Johnson
审校|617
编辑|豫小鱼


