编者按:
表观遗传组的失调会驱动异常的转录程序,促进癌症等疾病的发生和进展。近年来,一些研究人员正在尝试从表观遗传学入手开发全新的疗法,以治疗不同的疾病。
今天,我们共同关注表观遗传疗法。希望本文能够为相关的产业人士和诸位读者带来一些启发和帮助。
当我们开始学习一门新技能时,我们总是从简到难,并且在开始时,往往局限于我们所尊重的框架。例如,在童年时期,我们通过在涂色书规定的图案内涂色来培养运动技能。然而,一旦我们对自己的运动技能有了信心,我们就可以变得更有创造力。
表观遗传疗法领域也在经历着类似的学习过程。最初,表观遗传疗法是严格的表观遗传疗法,也就是说,表观遗传靶点是孤立的,而表观遗传疗法则针对这些孤立靶点采取行动。可惜的是,这样的表观遗传疗法带来的结果是参差不齐且有限的。最终,药物开发人员认识到表观遗传疗法在联合治疗中可能能够起到更好的效果。
而现在,随着药物应用范围的扩大,药物开发人员逐渐意识到表观遗传疗法越来越微妙以及强大的效果——包括更真实的效果,这些药物甚至还反映了一种新的先进性,一种对靶点进行巧妙处理而非打击它们的能力——表观遗传疗法可以使功能失调的细胞恢复健康,而不是破坏它们。
图. CellCentric 公司研究了超过 50 个潜在的表观遗传相关药物靶点,然后才专注于研究 P300/CBP。
“表观遗传药物(epigenetic drug)这个术语并不一定正确,”CellCentric 公司的首席执行官 Will West 博士说,“有许多药物含有与表观遗传相关的成分,但它们是否真的以表观遗传的方式作用还不清楚。”West 认为药物可能在产生表观遗传效应的同时,还会产生其他效应。
CellCentric 公司的主要候选治疗药物 CCS1477 正是这样一种药物。它具有表观遗传和细胞信号转导双重效应,因为它的靶点是影响癌症驱动基因表达以及癌症相关关键信号转导途径的组蛋白乙酰转移酶 P300 及其旁系同源蛋白 CREB 结合蛋白(CBP)。
具体地,P300 和 CBP 作为转录共激活因子,触发与肿瘤进展相关的某些基因的表达,如 c-Myc、AR 和 IRF4。这些蛋白质还能阻止重要信号蛋白的乙酰化,并使信号蛋白发生泛素化和降解。
使用 CCS1477, CellCentric 公司的科学家首次表明,P300/CBP 可以靶向阻断雄激素受体途径的信号转导。
CCS1477 是一种选择性小分子溴结构域抑制剂。实验表明,CCS1477 对特定癌细胞系和多个患者衍生异种移植模型具有效力,并成为了第一个进入临床试验的 P300/CBP 抑制剂。I期临床试验的肿瘤活检结果表明,CCS1477 具有靶向活性。
West 指出:“靶向表观遗传相关的作用机制与靶向特定受体或降解特定的蛋白质是不同的”。如果两种疗法的作用机制是不同的,那么我们就可以将两种疗法结合使用,以发挥协同效益。
“我们已经看到了全面的协同效应,” West 肯定地说道,“无论是与影响雄激素受体的前列腺癌第二代抗激素药物联合使用,还是与用于治疗受 MYC 和 IRF4 影响的血液恶性肿瘤的标准护理药物联合使用,都出现了这种协同效应。”
最近,一项大型、多机构合作研究进行了 shRNA 筛选,结果显示,CCS1477 和其他 P300/CBP 抑制剂协同增强了细胞对氮杂胞苷的反应,氮杂胞苷是目前高危骨髓增生异常综合征患者的最佳治疗选择。
除了前列腺癌和血液恶性肿瘤,CellCentric 公司的科学家们预计,CCS1477 还可以用于具有特定致癌因子过表达情况的肿瘤,如小细胞肺癌、乳腺癌和膀胱癌。
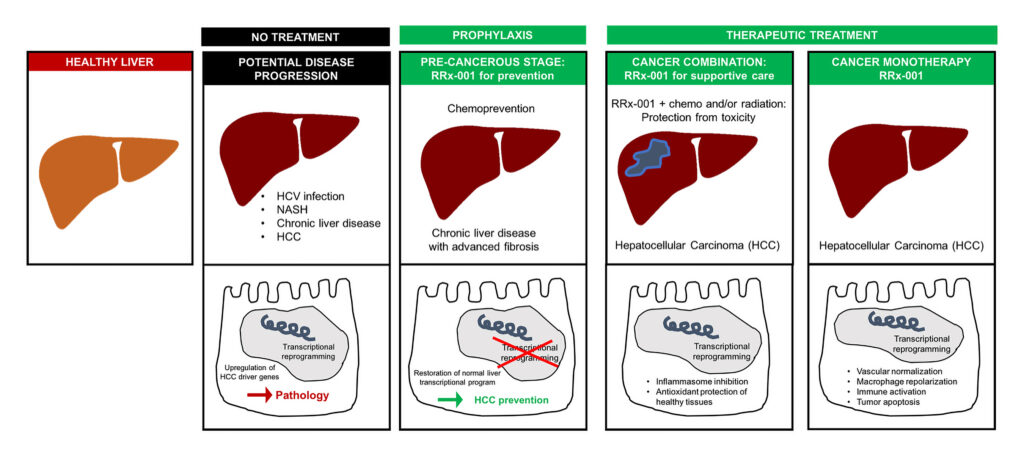
图. EpicentRx 公司正在开发 RRx-001 药物。
EpicentRx 公司的首席医疗官 Bryan Oronsky 博士表示,当今,大多数新药物都是现有药物的再利用或改良版。这种观点可能解释了为什么 EpicentRx 公司开始在药物行业之外寻找灵感。
最终,该公司发现,一种来自国防工业的新型分子结构具有治疗潜力。通过调整新型分子结构,EpicentRx 公司希望开发出新的治疗药物,用 Oronsky 的话来说就是“提供新的和尚未开发的作用机制”。
这种来自国防工业领域的小分子被命名为 RRx-001,正处于治疗几种恶性肿瘤的III期试验,以及抑制伴随几种慢性疾病的异常炎症的临床前研究。
源自国防工业领域的分子具有某些优势。例如,许多这样的分子已经进行过毒性评估,包括对动植物的毒性作用。这就意味着这些分子可以在确保安全性的情况下进入临床研究。
虽然基于靶点的筛选是药物发现中最常用的方法,但 EpicentRx 公司选择使用表型筛选来评估 RRx-001 和其他一些分子。“我们不知道这些分子会做什么或如何做,但我们感觉它们会使细胞敏感,因为它们的作用机制,” Oronsky 说,“事实证明,RRx-001 是一种放射增敏剂。”
EpicentRx 公司的研究发现,RRx-001 通过几种不同的分子机制发挥作用。该化合物具有免疫治疗活性;它将M2型巨噬细胞逆转为具有抗肿瘤活性的M1型巨噬细胞;它激活了抗氧化信号通路;它使癌细胞对此前已经无响应的疗法重新变得敏感。
“RRx-001 还具有表观遗传特性,”Oronsky 补充道,“我们看到它抑制了 DNA 甲基转移酶和组蛋白去乙酰化酶,并激活了 sirtuins 蛋白。” 这些调控表观遗传学的机制使 RRx-001 在改变表观遗传修饰的现有药物中处于独特的地位。
EpicentRx 还评估了 RRx-001 是否会使健康细胞对放射的敏感性增强。意想不到的是,EpicentRx 公司发现 RRx-001 实际上对健康细胞有保护作用。
“在接受全身辐照的小鼠中,RRx-001 保护了肠隐窝干细胞免受辐射的毒性,”Oronsky 指出,“而且 RRx-001 逆转或降低了化疗对健康组织的毒性。”从安全角度来看,这使得 RRx-001 特别有价值。
对于以全基因组方式调节表观遗传途径的化合物来说,毒性是一个特别严重的问题,并且有可能在无意之中改变基因表达。Oronsky 说:“表观遗传疗法的未来可能是对表观基因组进行编辑。”
“我们正在致力于研究将催化活性不强的 Cas9 融合到 RRx-001 中,以便我们能够使靶基因的特定启动子区域去甲基化,”Oronsky 说,“我们希望获得阻止转录和沉默基因的能力。”

大多数表观遗传疗法的开发者都专注于选择性地杀死功能失调的细胞。然而,一家名为 Durect 的公司正在探索另一种方法。Durect 公司专注于消除导致细胞功能失调的表观遗传缺陷。按照这种思路,Durect 公司打算开发能够治疗急性器官损伤和慢性肝病的药物。
DUR-928 是 Durect 公司的主要候选药物。它是一种内源性硫酸化氧甾醇,可抑制 DNMT1、DNMT3a 和 DNMT3b 这三种存在于哺乳动物体内的 DNA 甲基转移酶,从而调节许多控制关键细胞活动的基因的表达。
DUR-928 正在进行临床开发,用于治疗酒精性肝炎(AH),一种高度致命的急性炎症性肝病。目前还没有疗法被批准用于治疗 AH,这是医疗和公共卫生领域面临的一个重大挑战。
AH 患者显示出 DNMT1 和 DNMT3a 水平的升高,并表现出许多基因的 DNA 高甲基化。根据 Durect 公司的研究,DUR-928 显著降低了这种异常的高甲基化,并有助于恢复与脂质代谢、炎症反应和细胞存活相关的基因表达。
最近完成的一项 IIa 期临床试验在第 1 天和第 4 天向中度或重度 AH 患者提供 DUR-928 输液。“19 名患者都活了下来,其中 14 人在接受第二剂治疗前就离开了医院,”Brown 说,“考虑到 AH 患者的 28 天总死亡率为 26%,我们认为这可能具有重要意义。”
继 IIa 期试验之后,一项规模更大的随机、双盲、安慰剂对照、国际多中心 IIb 期临床试验 AHFIRM 研究正在评估 DUR-928 对重症 AH 患者的安全性和有效性。
溴结构域和末端外结构域(BET)蛋白抑制剂是一类重要的表观遗传抗癌药物。它们早在 20 世纪 90 年代初就被发现了,但直到过去十年才因其治疗潜力而引起了研究人员的密切关注。
尽管它们被发现可以选择性地干扰肿瘤细胞中的基因表达,但 BET 抑制剂并没有显示出太多的单药活性。这一缺陷在一些评估 BET 抑制剂对血液恶性肿瘤和实体瘤的疗效的临床试验中尤为突出。
不过,临床前数据显示,BET 抑制剂与其他药物联合使用可能会有效。Zenith Epigenetics 公司的首席商务官 Sanjay Lakhotia 博士宣称:“我们的信念始终是组合,我们启动了与小分子 BET 抑制剂的联合研究,以调节对现有疗法的耐药性。”
ZEN-3694 是 Zenith 公司研发的主要治疗化合物,目前正被用于精准肿瘤市场的多种组合方案中。Zenith 公司战略的一个关键重点是确定对特定组合做出最佳反应的患者亚群。
Lakhotia 直言:“我们的药物是第一个在两种不同类型的实体瘤中都显示出临床疗效的药物。”
Zenith 公司的科学家在一项 Ib/II 期剂量增加/扩展研究中,评估了 ZEN-3694 联合 enzalutamide(恩杂鲁胺,一种雄激素受体抑制剂,由安斯泰来制药和辉瑞公司开发)治疗转移性去势抵抗性前列腺癌的安全性和有效性。
该组合显示出了显著的治疗效果,特别是对 abiraterone(阿比特龙)反应不佳且有可能成为雄激素受体非依赖性的参与者。
另一个药物组合项目是 ZEN-3694 和辉瑞公司的 PARP 抑制剂 talazoparib 联合用于治疗局部晚期或转移性三阴性乳腺癌患者。此前,单独使用 talazoparib 已被证明有利于延长晚期乳腺癌和生殖系 BRCA1/2 突变患者的无进展生存期,但该药物对野生型 BRCA1/2 肿瘤的疗效非常有限。而 ZEN-3694 与 talazoparib 联合使用则可以显著提高这类患者的临床反应率。

专注于肿瘤学的 Zenith Epigenetics 公司的 BET 抑制技术起源于 BET 表观遗传学的先驱——Resverlogix 公司。早在 2013 年,Zenith 公司就从致力于心血管疾病的 Resverlogix 公司剥离出来,而如今,Resverlogix 公司则继续专注于肿瘤学领域以外的慢性疾病。除了寻找治疗心血管疾病的方法外,该公司还在开发治疗糖尿病、慢性肾病和代谢性疾病的药物。
Resverlogix 公司的主要候选药物是 apabtalone(RVX-208),这是一种口服小分子 BET 抑制剂,可选择性调节 BRD4 (BD2)。Apabetalone 可降低心血管疾病中的全身炎症标志物,改善慢性肾病患者的内皮功能障碍和动脉粥样硬化,并在体外水平上减轻 SARS-CoV-2 感染,其水平与抗病毒药物相当。这些作用是通过抑制由促炎刺激触发的 BET 介导的转录而起效的。
Resverlogix 公司和 Zenith 公司的总裁兼首席执行官 Donald McCaffrey 说:“我们已经看到,无论患者患有糖尿病、肾病或心血管疾病,BRD4 都会被招募到基因组中,并使其靶向的基因保持开启的状态。”作为一种选择性溴结构域抑制剂,apabtalone 可以抑制 BRD4 与其分子靶点的结合,并使慢性疾病发病机制中异常的表观遗传变异正常化。
“在表观遗传疗法中,我们不想打击靶点,”McCaffrey 解释说,“我们只想给靶点挠挠痒。”
许多正在开发的疗法都试图调节疾病中单个蛋白质的细胞水平。McCaffrey 指出:“这只对由单一蛋白质变化引起的疾病有效。”许多人类疾病,包括心血管疾病、糖尿病、慢性肾脏疾病和痴呆症,都是复杂而多面化的。因此,它们并不适合使用针对单一蛋白质的干预措施。
McCaffrey 强调说:“这些病症中的每一种情况都是许多个蛋白质和整个途径失调的结果。”在这些复杂的病症中,转录失调往往是由内部或外部环境的改变而造成的,如饮食或病毒感染,并可通过 BET4 的抑制来纠正。
Resverlogix 公司的科学家们不仅在研究将 apabetalone 作为单药使用对抗复杂疾病,同时也在探索该药物与其他疗法联合使用的效果。
“我们正在研究将 apabetalone 与几种现有药物联合使用,包括他汀类药物、β-受体阻滞剂和 ACE 抑制剂。”McCaffrey 介绍道。
Resverlogix 公司发现,apabetalone 与某些抗糖尿病治疗药物联合使用可能特别有效,特别是钠-葡萄糖共转运体-2(SGLT2)抑制剂或二肽基肽酶 4(DPP4)抑制剂。Apabetalone 与 SGLT2 或 DPP4 抑制剂联合使用,比单独使用 SGLT2 或 DPP4 抑制剂更能改善肾功能指标,并会更有效地降低主要不良心血管事件的风险。
原文链接:
https://www.genengnews.com/topics/translational-medicine/epigenetic-therapies-start-operating-outside-the-lines/
作者|Richard A. Stein
编译|竹夭
审校|617
编辑|豫小鱼


